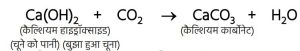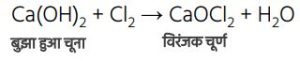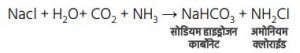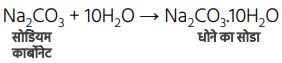कक्षा 10 विज्ञान अध्याय 2 – अम्ल, क्षारक और लवण
| अम्ल | क्षार |
|---|---|
| स्वाद में खट्टे होते हैं | स्वाद में कड़वे होते हैं |
| नीले लिटमस पत्र को लाल कर देते हैं | लाल लिटमस पत्र को नीला कर देते हैं |
| जलीय विलयन में H⁺ आयन देते हैं | जलीय विलयन में OH⁻ आयन देते हैं |
| उदाहरण: | उदाहरण: |
| HCl – हाइड्रोक्लोरिक अम्ल | NaOH – सोडियम हाइड्रॉक्साइड |
| H₂SO₄ – सल्फ्यूरिक अम्ल | KOH – पोटेशियम हाइड्रॉक्साइड |
| HNO₃ – नाइट्रिक अम्ल | Ca(OH)₂ – कैल्शियम हाइड्रॉक्साइड |
| CH₃COOH – ऐसिटिक अम्ल | NH₄OH – अमोनियम हाइड्रॉक्साइड |
लिटमस विलयन –
- यह बैंगनी रंग का रंजक होता है।
- इसे थैलोफाइटा समूह के लिचेन पौधे से निकाला जाता है।
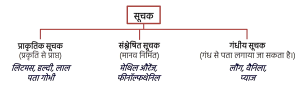
सूचक –
- पदार्थ की अम्लीय व क्षारीय प्रकृति की पहचान करने में उपयोग आने वाले पदार्थ।
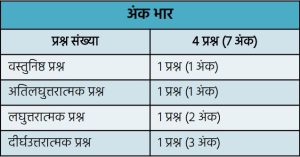
बहुचयनात्मक प्रश्न / रिक्त स्थान
1. निम्नलिखित में से प्राकृतिक सूचक है —
(अ) हल्दी (ब) प्याज (स) लौंग (द) नील
उत्तर : (अ) हल्दी
2. लिटमस एक किस वर्ग के पादप से प्राप्त किया जाता है —
(अ) टेरिडोफाइटा (ब) थैलोफाइटा (स) ब्रायोफाइटा (द) स्पर्मेटोफाइटा
उत्तर : (ब) थैलोफाइटा
3. दही में उपस्थित अम्ल है — (2024)
(अ) ऑक्सैलिक अम्ल (ब) टारटारिक अम्ल (स) मेथेनोइक अम्ल (द) लैक्टिक अम्ल
उत्तर : (द) लैक्टिक अम्ल
4. सिरका में उपस्थित अम्ल का रासायनिक नाम ___________ है। (2023)
उत्तर : एसीटिक अम्ल
अतिलघुत्तरात्मक प्रश्न
- टमाटर व चींटी के डंक में कौन-सा अम्ल पाया जाता है? (2023)
- संतरे में पाए जाने वाले अम्ल का नाम लिखिए। (2022)
- स्वाद के आधार पर अम्ल व क्षार में अंतर लिखिए। (2022)
- गंधीय सूचक का कोई एक उदाहरण लिखिए। (2023)
अतिलघुत्तरात्मक प्रश्नों के हल
1.(a) टमाटर में ऑक्सैलिक अम्ल पाया जाता है।
(b) चींटी के डंक में मेथेनोइक अम्ल पाया जाता है।
2. सिट्रिक अम्ल – यह अम्ल नींबू, संतरा और अन्य खट्टे फलों में पाया जाता है।
3.
अम्ल (Acids): स्वाद में खट्टे होते हैं।
क्षार (Bases): स्वाद में कड़वे होते हैं।
4.
कुछ पदार्थों की गंध अम्लीय या क्षारकीय माध्यम में बदल जाती है।
ऐसे सूचकों को गंधीय (Olfactory) सूचक कहा जाता है।
उदाहरण: वैनिला, प्याज तथा लौंग का तेल
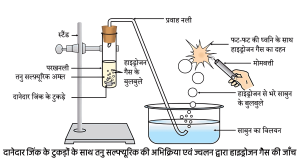
1. अम्ल एवं क्षारक की धातु के साथ अभिक्रिया –
➢ अम्ल + धातु → लवण + हाइड्रोजन गैस
उदाहरण-
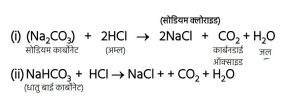
2. अम्ल की धातु कार्बोनेट तथा धातु हाइड्रोजन कार्बोनेट के साथ अभिक्रिया –
➢ अम्ल + धातु कार्बोनेट / धातु हाइड्रोजन कार्बोनेट → लवण + कार्बन डाइऑक्साइड + जल
उदाहरण –
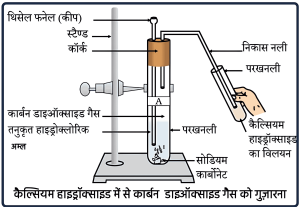
3. बुझा हुए चूने का परीक्षण –
कार्बन डाइऑक्साइड को चूने के पानी में प्रवाहित करने पर पानी दूधिया (दूध जैसा सफेद) हो जाता है।
उदाहरण –
अधिक मात्रा में CO₂ प्रवाहित करने पर –
उदाहरण –
वह अभिक्रिया जिसमें अम्ल व क्षार परस्पर क्रिया कर लवण व जल बनाते हैं।
➢ अम्ल + क्षार → लवण + जल
उदाहरण –
HCl + NaOH → NaCl + H₂O
क्षार :
जल में घुलनशील क्षारक को क्षार कहते हैं।
तनुकरण :
जल में अम्ल या क्षार मिलाने की प्रक्रिया को तनुकरण कहते हैं।
इस प्रक्रिया में आयनों (H⁺ / OH⁻) की सांद्रता प्रति इकाई आयतन घट जाती है।
4. अम्लों की धात्विक ऑक्साइडों के साथ अभिक्रिया –
➢ धातु ऑक्साइड + अम्ल → लवण + जल
धातु ऑक्साइड को क्षारकीय ऑक्साइड भी कहते हैं।
उदाहरण –
5. क्षारक की अधात्विक ऑक्साइड के साथ अभिक्रिया –
➢ अधातु ऑक्साइड + क्षार → लवण + जल
अम्ल जलीय विलयन में H⁺ आयन देते हैं तथा क्षार जलीय विलयन में OH⁻ आयन देते हैं।
चूंकि विलयन में विद्युत धारा का प्रवाह आयनों द्वारा होता है, इसलिए अम्ल व क्षार, आयन देने के कारण विद्युत के चालक होते हैं।
उदाहरण –
प्रबल अम्ल
जो अत्यधिक संख्या में H⁺ आयन देते हैं।
उदाहरण – HCl, H₂SO₄, HNO₃
दुर्बल अम्ल
जो कम संख्या में H⁺ आयन देते हैं।
उदाहरण – CH₃COOH
प्रबल क्षार
जो अधिक संख्या में OH⁻ आयन देते हैं।
उदाहरण – NaOH, KOH
दुर्बल क्षार
जो कम संख्या में OH⁻ आयन देते हैं।
उदाहरण – NH₄OH, Ca(OH)₂, Mg(OH)₂
Mg(OH)₂ → मिल्क ऑफ मैग्नीशिया (पेट की अम्लता को दूर करता है)
बहुचयनात्मक प्रश्न
निम्न में दुर्बल अम्ल है-
(अ) HCI
(ब) H₂SO₄
(स) CH₃COOH
(द) HNO₃चूने के पानी से कौनसी गैस प्रवाहित करने पर यह दुधिया हो जाता है-
(अ) H₂
(ब) CO₂
(स) CO
(द) H₂अम्ल धातु से क्रिया करके प्रदान करते है-
(अ) विरंजक चूर्ण
(ब) धातु कार्बोनेट
(स) लवण तथा हाइड्रोजन
(द) धातु ऑक्साइडकोई विलयन अंडे के पिसे हुए कवच से अभिक्रिया कर एक गैस उत्पन्न करता है जो चूने के पानी को दुधिया कर देती है। इस विलयन में क्या होगा?
(अ) NaCl
(ब) HCI
(स) LiCl
(द) KCINaOH का 10 mL विलयन, HCI के 8 ml विलयन से पूर्णतः उदासीन हो जाता है। यदि हम NaOH के उसी विलयन का 20 ml लें तो इसे उदासीन करने के लिए HCI के उसी विलयन की कितनी मात्रा की आवश्यकता होगी?
(अ) 4 ml
(स) 12 ml
(ब) 8 ml
(द) 16 ml
अतिलघुत्तरात्मक प्रश्न
बुझा हुआ चुने का रासायनिक सूत्र लिखिए।
किन्ही दो दुर्बल क्षारों के नाम उनके रासायनिक सूत्र के साथ लिखिए।
कॉपर सल्फेट का रासायनिक सूत्र लिखिए।
उदासीनीकरण अभिक्रिया को परिभाषित कीजिए। (2023)
अम्ल के जलीय विलयन द्वारा विद्युत के संचालन का नामांकित चित्र बनाइये। (2022)
अतिलघुत्तरात्मक प्रश्न के हल
बुझा हुआ चुना – Ca(OH)₂
दुर्बल क्षार –
NH₄OH – अमोनियम हाइड्रॉक्साइड
Ca(OH)₂ – कैल्शियम हाइड्रॉक्साइड
CuSO₄·5H₂O
अम्ल एवं क्षार की अभिक्रिया के परिणामस्वरूप लवण तथा जल प्राप्त होता है, इसे उदासीनीकरण अभिक्रिया कहते हैं।
उदाहरण – HCl(aq) + NaOH(aq) → NaCl(aq) + H₂O
लघुत्तरात्मक प्रश्न
पीतल एवं तांबे के बर्तनों में दही एवं खट्टे पदार्थ क्यों नहीं रखने चाहिए?
टिप्पणी लिखिए –
a. उदासीनीकरण अभिक्रिया
b. प्रबल अम्ल व दो उदाहरणअम्ल व क्षार में समानता उदाहरण सहित समझाइए।
भस्मित जल विद्युत का चालक क्यों नहीं होता, जबकि वर्षा जल होता है?
अम्ल तथा क्षार की धातु के साथ रासायनिक अभिक्रिया लिखिए।
चूने के पानी में कार्बन डाइऑक्साइड गैस को प्रवाहित करने पर यौगिक [A] का अवक्षेप बनता है। यदि इसमें अधिक मात्रा में कार्बन डाइऑक्साइड गैस को प्रवाहित किया जाए तो एक जल में घुलनशील पदार्थ [B] बनता है। [A] व [B] के रासायनिक सूत्र तथा निहित रासायनिक अभिक्रियाओं के समीकरण लिखिए। (2023)
जल की अनुपस्थिति में अम्ल का व्यवहार अम्लीय क्यों नहीं होता है?
निम्न अभिक्रियाओं के लिए पहले शब्द-समीकरण लिखिए तथा उसके बाद संतुलित समीकरण –
(A) तनु सल्फ्यूरिक अम्ल दानेदार जिंक के साथ अभिक्रिया करता है।
(B) तनु हाइड्रोक्लोरिक अम्ल मैग्नीशियम पट्टी के साथ अभिक्रिया करता है।
(C) तनु सल्फ्यूरिक अम्ल ऐलुमिनियम चूर्ण के साथ अभिक्रिया करता है।
(D) तनु हाइड्रोक्लोरिक अम्ल लौह के रजतन के साथ अभिक्रिया करता है।अम्ल की धात्विक ऑक्साइड के साथ अभिक्रिया उदाहरण सहित समझाइए।
अम्ल का जलीय विलयन विद्युत का चालन क्यों करता है?
शुष्क हाइड्रोक्लोरिक गैस शुष्क लिटमस पत्र का रंग क्यों नहीं बदलती है?
अम्ल को तनु करते समय यह क्यों अनुशंसित किया जाता है कि अम्ल को जल में मिलाना चाहिए, न कि जल को अम्ल में?
जब सोडियम हाइड्रॉक्साइड विलयन में अधिक मात्रा में क्षारक मिलाते हैं तो हाइड्रॉक्साइड आयन (OH⁻) की सांद्रता कैसे प्रभावित होती है?
लघुत्तरात्मक प्रश्न के हल
दही और खट्टे पदार्थों को पीतल या तांबे के बर्तनों में नहीं रखना चाहिए क्योंकि दही व अन्य खट्टे खाद्य पदार्थों में अम्ल होते हैं, जो धातु (पीतल व तांबा) के बर्तनों से अभिक्रिया कर जहरीले धातु यौगिक बनाते हैं। ये यौगिक भोजन को विषैला बना देते हैं और हमारे स्वास्थ्य पर प्रतिकूल प्रभाव डालते हैं।
a. उदासीनीकरण अभिक्रिया –
यह वह अभिक्रिया है जिसमें अम्ल और क्षार परस्पर क्रिया कर लवण व जल बनाते हैं।
उदाहरण: HCl + NaOH → NaCl + H₂O(b) प्रबल अम्ल –
(a) H₂SO₄ – सल्फ्यूरिक अम्ल
(b) HNO₃ – नाइट्रिक अम्लअम्ल जलीय विलयन में H⁺ आयन देते हैं तथा क्षार जलीय विलयन में OH⁻ आयन देते हैं। चूंकि विलयन में विद्युत धारा का प्रवाह आयनों द्वारा होता है, इसलिए अम्ल व क्षार, आयन देने के कारण विद्युत के चालक होते हैं।
उदाहरण:
HCl + H₂O → H₃O⁺ + Cl⁻
NaOH → Na⁺ + OH⁻आसुत जल शुद्ध होता है, जिसमें कोई आयन नहीं होते हैं, इसलिए यह विद्युत का चालन नहीं करता।
वर्षा के जल में थोड़ी मात्रा में अम्ल होते हैं क्योंकि वायु में उपस्थित CO₂ और NO₂ गैसें जल में मिलकर इसे अम्लीय बना देती हैं। ये अम्ल (H⁺) आयन उत्पन्न करते हैं, जिसके कारण वर्षा का जल विद्युत धारा का चालन कर पाता है।अम्ल एवं क्षारक की धातु के साथ अभिक्रिया –
अम्ल या क्षार धातु से अभिक्रिया कर लवण और हाइड्रोजन गैस बनाते हैं।
उदाहरण:
2HCl + Zn → ZnCl₂ + H₂
2NaOH + Zn → Na₂ZnO₂ + H₂चूने के पानी में CO₂ गैस प्रवाहित करने पर कैल्सियम कार्बोनेट (CaCO₃) का श्वेत अवक्षेप बनता है।
यदि इसमें अधिक मात्रा में CO₂ गैस प्रवाहित की जाए, तो कैल्सियम बाइकार्बोनेट [Ca(HCO₃)₂] बनता है, जो जल में घुलनशील होता है।
रासायनिक समीकरण:
Ca(OH)₂(aq) + CO₂(g) → CaCO₃(s) + H₂O(l)
CaCO₃(s) + H₂O(l) + CO₂(g) → Ca(HCO₃)₂(aq)अम्ल अपने अम्लीय गुण H⁺(aq) आयनों के कारण दिखाते हैं। जल की अनुपस्थिति में अम्ल आयनित नहीं होते तथा H⁺(aq) आयन नहीं देते, इसलिए वे अम्लीय व्यवहार नहीं करते हैं।
(अ) तनु सल्फ्यूरिक अम्ल दानेदार जिंक के साथ अभिक्रिया करता है –
शब्द समीकरण: जिंक + तनु सल्फ्यूरिक अम्ल → जिंक सल्फेट + हाइड्रोजन गैस
रासायनिक समीकरण: Zn(s) + H₂SO₄(aq) → ZnSO₄(aq) + H₂(g)(ब) तनु हाइड्रोक्लोरिक अम्ल मैग्नीशियम पट्टी के साथ अभिक्रिया करता है।
मैग्नीशियम + तनु हाइड्रोक्लोरिक अम्ल → मैग्नीशियम क्लोराइड + हाइड्रोजन गैस
Mg(s) + 2HCl(aq) → MgCl₂(aq) + H₂(g)(स) तनु सल्फ्यूरिक अम्ल ऐलुमिनियम चूर्ण के साथ अभिक्रिया करता है।
ऐलुमिनियम + तनु सल्फ्यूरिक अम्ल → ऐलुमिनियम सल्फेट + हाइड्रोजन गैस
2Al(s) + 3H₂SO₄(aq) → Al₂(SO₄)₃(aq) + 3H₂(g)(द) तनु हाइड्रोक्लोरिक अम्ल लौह के रेतन के साथ अभिक्रिया करता है।
लोहा + तनु हाइड्रोक्लोरिक अम्ल → फेरस क्लोराइड + हाइड्रोजन गैस
Fe(s) + 2HCl(aq) → FeCl₂(aq) + H₂(g)
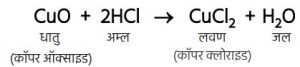
- धातु ऑक्साइड अम्ल के साथ अभिक्रिया कर लवण व जल बनाते हैं।
धातु ऑक्साइड इस तरह क्षारक की तरह व्यवहार करता है, जिस कारण ये ऑक्साइड क्षारकीय ऑक्साइड भी कहलाते हैं।
उदाहरण –
CuO + 2HCl → CuCl₂ + H₂O
(कॉपर ऑक्साइड) (कॉपर क्लोराइड)
- अम्ल, जलीय विलयन में विघटित होकर आयन बनाते हैं।
ये आयन विद्युत के संचालन के लिए जिम्मेदार होते हैं।
- लिटमस पत्र का रंग हाइड्रोजन आयनों द्वारा बदला जाता है।
शुष्क HCl गैस में H⁺ आयन नहीं होते हैं।
केवल जलीय विलयन में ही अम्ल आयनों में विघटित होते हैं।
अतः शुष्क लिटमस पत्र का रंग परिवर्तित नहीं होता है।
- अम्ल को जल में मिलाने की प्रक्रिया ऊष्माक्षेपी होती है,
इसलिए यह हमेशा अनुशंसा की जाती है कि अम्ल को पानी में मिलाया जाए, न कि पानी को अम्ल में।
यदि अम्ल में जल मिलाया जाएगा तो बड़ी मात्रा में ऊष्मा के उत्सर्जन के कारण अम्ल की कुछ बूंदें चेहरे या कपड़ों पर आ सकती हैं, जिससे क्षति होने का खतरा बढ़ जाता है।
- जब सोडियम हाइड्रॉक्साइड (NaOH) के घोल में अतिरिक्त क्षार मिलाया जाता है,
तो OH⁻ आयनों की सान्द्रता में वृद्धि होती है।
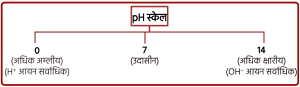
➢ यह विलयन में H⁺ आयन एवं OH⁻ आयन की सांद्रता बताता है।
➢ इसका मान 0 से 14 तक होता है।
अम्लीय वर्षा —
➢ जब वर्षा के जल की pH 5.6 से कम हो।
दंत क्षय —
➢ जब मुँह के pH का मान 5.5 से कम हो।
➢ दाँतों का इनैमल कैल्सियम फॉस्फेट [Ca₃(PO₄)₂] से बना होता है, जो शरीर का सबसे कठोर पदार्थ है।
➢ मुँह का pH 5.5 से कम होने पर इनैमल नष्ट होने लगता है।
याद रखें —
| पदार्थ | pH मान |
|---|---|
| जठर रस | 1.2 |
| नींबू रस | 2.2 |
| ताजा दूध | 6 |
| शुद्ध जल | 7 |
| रक्त | 7.4 |
| मिल्क ऑफ मैग्नेशिया | 10 |
| सोडियम हाइड्रॉक्साइड | 14 |
| शरीर की pH परास | 7 – 7.8 |
| प्राकृतिक स्रोत | अम्ल का नाम |
|---|---|
| सिरका | एसीटिक अम्ल |
| संतरा | साइट्रिक अम्ल |
| चींटी का डंक | मिथेनोइक अम्ल |
| दही | लैक्टिक अम्ल |
| इमली | टार्टरिक अम्ल |
| टमाटर | ऑक्सैलिक अम्ल |
बहु-विकल्पीय प्रश्न (MCQs)
- उदासीन विलयन का pH मान होगा —
(अ) 0 (ब) 7 (स) 10 (द) 14 (उत्तर: ब) - ताजे दूध का pH मान होता है —
(अ) 4 (ब) 5 (स) 6 (द) 7 (उत्तर: स) - कोई विलयन लाल लिटमस को नीला कर देता है, इसका pH संभवतः क्या होगा?
(अ) 1 (ब) 4 (स) 5 (द) 10 (उत्तर: द) - अपच का उपचार करने के लिए निम्न में से किस औषधि का उपयोग होता है?
(अ) एंटीबायोटिक (प्रतिजैविक)
(ब) एनाल्जेसिक (पीड़ाहर)
(स) एंटासिड
(द) एंटीसेप्टिक (प्रतिरोधी) (उत्तर: स) - अगर किसी विलयन का pH 7 से अधिक है, इसका अर्थ है कि उस विलयन में —
(अ) हाइड्रोजन आयन की संख्या अधिक है।
(ब) हाइड्रॉक्साइड आयन की संख्या अधिक है।
(स) हाइड्रॉक्साइड आयन की संख्या कम है।
(द) हाइड्रोजन और हाइड्रॉक्साइड आयन दोनों बराबर हैं। (उत्तर: ब)
अति लघुत्तरात्मक प्रश्न
- अम्लीय वर्षा का pH मान कितना होता है?
उत्तर: जब वर्षा के जल का pH 5.6 से कम हो, तो वह वर्षा अम्लीय वर्षा कहलाती है।
लघुत्तरात्मक प्रश्न
- आपके पास दो विलयन ‘A’ एवं ‘B’ हैं। विलयन ‘A’ के pH का मान 6 है तथा विलयन ‘B’ के pH का मान 8 है। किस विलयन में हाइड्रोजन आयन की सांद्रता अधिक है? इनमें से कौन अम्लीय है तथा कौन क्षारकीय?
उत्तर: 7 से कम pH मान अम्लीय विलयन को इंगित करता है, जबकि 7 से अधिक pH मान क्षारकीय विलयन को। चूंकि विलयन A का pH 6 है, अतः इसमें H⁺ आयनों की सांद्रता अधिक है। इसलिए, विलयन A अम्लीय है और विलयन B (pH 8) क्षारकीय है। - H⁺ (aq) आयन की सांद्रता का विलयन की प्रकृति पर क्या प्रभाव पड़ता है?
उत्तर: H⁺ आयनों की सांद्रता जितनी अधिक होगी, विलयन की अम्लीय प्रकृति उतनी ही अधिक होगी। - क्या क्षारकीय विलयन में H⁺ (aq) आयन होते हैं? अगर हाँ, तो ये क्षारकीय क्यों होते हैं?
उत्तर: हाँ, क्षारकीय विलयनों में H⁺ (aq) आयन उपस्थित होते हैं, परंतु इनमें OH⁻ आयनों की संख्या H⁺ आयनों की तुलना में बहुत अधिक होती है, जो उनकी क्षारकीय प्रकृति के लिए उत्तरदायी है।

कुछ लवणों की सामान्य अभिक्रियाएँ —
साधारण नमक (NaCl):
सोडियम हाइड्रॉक्साइड (NaOH):
➢ इसे क्लोर-क्षार प्रक्रिया कहते हैं।
उपयोग: धातुओं से ग्रीस हटाने, साबुन तथा अपमार्जक में।
विरंजक चूर्ण (CaOCl₂) —
उपयोग: कपड़ों के विरंजन में।
➢ जल में रोगाणुनाशक के रूप में।
कॉपर सल्फेट का रासायनिक सूत्र: CuSO₄·5H₂O
स्फटिकीकरण का जल (Water of Crystallization):
➢ लवण के एक सूत्र इकाई में जल के निश्चित अणुओं की संख्या को स्फटिकीकरण का जल कहते हैं।
उदाहरण: कॉपर सल्फेट में स्फटिकीकरण जल के 5 अणु होते हैं।
CuSO₄·5H₂O
बेकिंग सोडा (NaHCO₃) —
उपयोग : खाने में।
➢ पेट की अम्लीयता दूर करने में।
धोने का सोड़ा (Na₂CO₃) —
उपयोग : काँच, साबुन, कागज उद्योग में।
➢ बोरेक्स (Na₂B₄O₇.10H₂O) उत्पादन में।
➢ जल की अस्थायी कठोरता दूर करने में।
प्लास्टर ऑफ पेरिस —
उपयोग : टूटी हुई हड्डियों को स्थिर करने में।
➢ खिलौना बनाने में।
| रासायनिक यौगिक का नाम | रासायनिक सूत्र |
|---|---|
| हाइड्रोक्लोरिक अम्ल | HCl |
| सल्फ्यूरिक अम्ल | H₂SO₄ |
| नाइट्रिक अम्ल | HNO₃ |
| ऐसिटिक अम्ल | CH₃COOH |
| सोडियम हाइड्रॉक्साइड | NaOH |
| कैल्शियम हाइड्रॉक्साइड / बुझा हुआ चूना | Ca(OH)₂ |
| पोटेशियम हाइड्रॉक्साइड | KOH |
| मैग्नीशियम हाइड्रॉक्साइड / मिल्क ऑफ मैग्नीशिया | Mg(OH)₂ |
| अमोनियम हाइड्रॉक्साइड | NH₄OH |
| रासायनिक यौगिक का नाम | रासायनिक सूत्र |
|---|---|
| कैल्शियम कार्बोनेट | CaCO₃ |
| सोडियम जिंकेट | Na₂ZnO₂ |
| सोडियम क्लोराइड (साधारण नमक) | NaCl |
| कॉपर क्लोराइड | CuCl₂ |
| विरंजक चूर्ण | CaOCl₂ |
| सोडियम हाइड्रोजन कार्बोनेट (खाने का सोड़ा / बेकिंग सोडा) | NaHCO₃ |
| धोने का सोडा | Na₂CO₃·10H₂O |
| जिप्सम | CaSO₄·2H₂O |
| प्लास्टर ऑफ पेरिस | CaSO₄·½H₂O |
| कॉपर सल्फेट | CuSO₄·5H₂O |
| बोरेक्स | Na₂B₄O₇·10H₂O |
बहुचयनात्मक प्रश्न
- POP का सूत्र है –
(अ) CuSO₄·½H₂O
(ब) CaSO₄·½H₂O
(स) CuSO₄·2H₂O
(द) CaSO₄·2H₂O
उत्तर – (ब) - निम्नलिखित में से किस पदार्थ में क्रिस्टलीय जल उपस्थित नहीं है? (2022)
(अ) धोने का सोडा
(ब) जिप्सम
(स) बेकिंग सोडा
(द) प्लास्टर ऑफ पेरिस
उत्तर – (स) - टूटी हुई हड्डियों को स्थिर करने तथा खिलौने निर्माण में किसका उपयोग किया जाता है?
(अ) प्लास्टर ऑफ पेरिस
(ब) धोने का सोडा
(स) सोडियम बाईकार्बोनेट
(द) सोडियम हाइड्रॉक्साइड
उत्तर – (अ)क प्रश्न
🧪 अतिलघुत्तरात्मक प्रश्न
- CaOCl₂ यौगिक का प्रचलित नाम क्या है?
- उस पदार्थ का नाम बताइए जो क्लोरीन से क्रिया करके विरंजक चूर्ण बनाता है।
- कठोर जल को मृदु करने के लिए किस सोडियम यौगिक का उपयोग किया जाता है?
- सोडियम हाइड्रोजनकार्बोनेट के विलयन को गर्म करने पर क्या होगा? इस अभिक्रिया के लिए समीकरण लिखिए।
🧾 अतिलघुत्तरात्मक प्रश्न के हल
- ब्लीचिंग पाउडर या विरंजक चूर्ण
- बुझा हुआ चूना (कैल्सियम हाइड्रॉक्साइड) Ca(OH)₂
Ca(OH)₂ + Cl₂ → CaOCl₂ + H₂O - सोडियम कॉर्बोनेट का उपयोग कठोर जल को मृदु करने के लिए किया जाता है।
- जब सोडियम हाइड्रोकार्बोनेट (सोडियम हाइड्रोजन कार्बोनेट) के घोल को गर्म किया जाता है, तो CO₂ गैस के निकलने के साथ सोडियम कार्बोनेट (Na₂CO₃) और जल (H₂O) का निर्माण होता है।
2NaHCO₃ → Na₂CO₃ + CO₂ + H₂O
लघुत्तरात्मक प्रश्न
- प्लास्टर ऑफ पेरिस को नमी-रोधी पात्र में क्यों रखा जाना चाहिए?
उत्तर:
प्लास्टर ऑफ पेरिस नमी के संपर्क में आने पर जल को अवशोषित कर जिप्सम (CaSO₄·2H₂O) में परिवर्तित हो जाता है तथा कठोर होकर जम जाता है।
इसलिए इसे जमने से बचाने के लिए नमी-रोधी बर्तन में रखा जाता है। - विरंजक चूर्ण का रासायनिक सूत्र व दो उपयोग लिखिए।
उत्तर:
रासायनिक सूत्र: CaOCl₂
उपयोग:
- (1) कपड़ों के विरंजन में
- (2) जल में रोगाणुनाशक के रूप में
- बोरेक्स में क्रिस्टलीय जल के कितने अणु होते हैं?
उत्तर: बोरेक्स में क्रिस्टलीय जल के 10 अणु होते हैं। - (1) प्लास्टर ऑफ पेरिस का रासायनिक सूत्र व उपयोग लिखिए।
(2) क्लोर-क्षार अभिक्रिया क्या है?
(3) धोने का सोडा और बेकिंग सोडा के दो-दो प्रमुख उपयोग लिखिए।
🧪 लघुत्तरात्मक प्रश्न के हल
1. प्लास्टर ऑफ पेरिस आर्द्रता के संपर्क में आने पर जल को अवशोषित कर जिप्सम में परिवर्तित हो जाता है तथा कठोर होकर जम जाता है। इसलिए इसे जमने से बचाने के लिए आर्द्र-रोधी बर्तन में रखा जाता है।
2.
(a) विरंजक चूर्ण – CaOCl₂
उपयोग –
(1) कपड़ों के विरंजन में।
(2) जल में रोगाणुनाशक के रूप में।
(b) बोरेक्स में क्रिस्टल जल के 10 अणु होते हैं।
3.
1. प्लास्टर ऑफ पेरिस – CaSO₄·½H₂O
उपयोग –
टूटी हुई हड्डियों को स्थिर करने में।
खिलौना बनाने में।
2. क्लोर क्षार अभिक्रिया — सोडियम क्लोराइड की जल से अभिक्रिया
3. धोने का सोडा — सोडियम कार्बोनेट की जल से अभिक्रिया कर धोने का सोडा बनता है।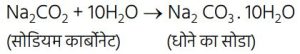
4. धोने का सोडा का उपयोग –
इसका उपयोग काँच, साबुन व कागज उद्योग में होता है।
यह धावन चूर्ण के घटक के रूप में प्रयोग होता है।
बैकिंग सोडा का उपयोग –
बैकिंग पाउडर के घटक के रूप में इसे बेकरी में प्रयोग में लाया जाता है।
यह प्रति-अम्लों के घटक के रूप में प्रयोग किया जाता है।
दीर्घउत्तरात्मक प्रश्न
(1) प्लास्टर ऑफ पेरिस – CaSO₄·½H₂O
उपयोग:
- टूटी हुई हड्डियों को स्थिर करने में
- खिलौने व सजावटी वस्तुएँ बनाने में
(2) क्लोर-क्षार अभिक्रिया:
सोडियम क्लोराइड की जल के साथ विद्युत अपघटन करने पर सोडियम हाइड्रॉक्साइड, क्लोरीन व हाइड्रोजन प्राप्त होते हैं।
समीकरण: 2NaCl + 2H₂O → 2NaOH + Cl₂ + H₂
(3) धोने का सोडा (Na₂CO₃·10H₂O):
- (i) यह काँच, साबुन एवं कागज़ उद्योग में प्रयोग किया जाता है।
- (ii) यह धावन पाउडर के घटक के रूप में प्रयोग होता है।
बेकिंग सोडा (NaHCO₃):
- (i) बेकिंग पाउडर के घटक के रूप में बेकरी में उपयोग किया जाता है।
- (ii) अम्लता के उपचार में प्रतिअम्ल (antacid) के रूप में प्रयोग किया जाता है।
दीर्घ उत्तरात्मक प्रश्न
- प्लास्टर ऑफ पेरिस का रासायनिक सूत्र लिखिए।
(i) जल मिलाने पर प्लास्टर ऑफ पेरिस कठोर क्यों हो जाता है?
उपयुक्त रासायनिक समीकरण देकर समझाइए। (2024) - बेकिंग सोडा का रासायनिक नाम लिखिए।
(i) केक मुलायम और स्पंजी क्यों हो जाता है?
उपयुक्त रासायनिक समीकरण देकर समझाइए। (2024) - सोडियम कार्बोनेट के साथ हाइड्रोक्लोरिक अम्ल की अभिक्रिया से यौगिक [A] बनता है।[A] को साधारण नमक भी कहते हैं।[A] के जलीय विलयन में विद्युत प्रवाहित करने पर सोडियम हाइड्रॉक्साइड बनता है।[A] का रासायनिक नाम तथा निहित रासायनिक अभिक्रियाओं के समीकरण लिखिए। (2023)
- निम्न सारणी के आधार पर पदार्थों की हाइड्रोजन आयन की सांद्रता घटते क्रम में लिखिए —
| पदार्थ | हाइड्रोजन आयन की सांद्रता (mol/L) |
|---|---|
| 1 | 22 |
| 2 | 176 |
| 3 | 4 |
| 4 | 12 |
| 5 | 44 |
- जब एक सोडियम यौगिक की अभिक्रिया HCl के साथ होती है, तब लवण, जल व एक गैस ‘Y’ प्राप्त होती है।
यह यौगिक ‘X’ केक (ब्रेड) को मुलायम व स्पंजी बनाने के लिए उपयोग होता है।
गैस ‘Y’ चूने के पानी को दुधिया (श्वेत अवक्षेप) बनाती है।
यौगिक ‘X’ व गैस ‘Y’ का नाम लिखिए। (2022)
दीर्घ उत्तरात्मक प्रश्न
(i) प्लास्टर ऑफ पेरिस का रासायनिक सूत्र — CaSO₄·½H₂O
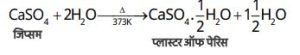
(ii) जिप्सम को 373 K पर गर्म करने पर यह जल के अणुओं का त्याग कर कैल्सियम सल्फेट अर्धहाइड्रेट या हैमिहाइड्रेट (CaSO₄·½H₂O) बनाता है, जिसे प्लास्टर ऑफ पेरिस कहते हैं।
यह एक सफेद चूर्ण है तथा इसमें जल मिलाने पर यह पुनः जिप्सम बनकर कठोर ठोस पदार्थ प्रदान करता है।
रासायनिक अभिक्रिया:
CaSO₄·2H₂O →(373 K)→ CaSO₄·½H₂O + 1½H₂O
(i) बेकिंग सोडा का रासायनिक नाम — सोडियम हाइड्रोजन कार्बोनेट (NaHCO₃)
(ii) जब बेकिंग सोडा को किसी अम्ल के साथ अभिक्रिया कराई जाती है, तो कार्बन डाइऑक्साइड गैस बनती है।
इस अभिक्रिया से उत्पन्न CO₂ के द्वारा पाव रोटी या केक में खमीर उठाया जा सकता है तथा ये मुलायम एवं स्पंजी हो जाते हैं।
रासायनिक अभिक्रिया:
NaHCO₃ + H⁺ → Na⁺ + CO₂ + H₂O
रासायनिक अभिक्रिया:
Na₂CO₃(s) + 2HCl(aq) → 2NaCl(aq) + CO₂(g) + H₂O(l)
(i) हाइड्रोजन आयन के लघुगणक को pH कहते हैं, जो किसी भी पदार्थ में उपस्थित H⁺ आयन की सांद्रता का माप है।
H⁺ आयन और pH में संबंध:
pH = -log[H⁺]
घटते क्रम में हाइड्रोजन आयन की सांद्रता:
3 > 1 > 2 > 4
(ii) NaHCO₃(s) + HCl(aq) → NaCl(aq) + H₂O(l) + CO₂(g)
यहाँ,
यौगिक X — NaHCO₃ (सोडियम हाइड्रोजन कार्बोनेट)
गैस Y — CO₂ (कार्बन डाइऑक्साइड)
RECENT POSTS
RRB Technician Grade 3 Result 2026 Out, Score Card Link
Mission Gyan2026-05-30T15:12:23+05:30May 30, 2026|0 Comments
RRB Technician Grade 3 Result 2026 Out The Railway Recruitment Board released the RRB Technician Grade 3 Result 2026 for different zones. Candidates who took the Technician Grade 3 CBT exam can now check their [...]
RRB Paramedical Score Card 2026 Out: Check Marks
Mission Gyan2026-05-30T13:26:51+05:30May 30, 2026|0 Comments
RRB Paramedical Score Card 2026 Out: Check Marks, Result PDF, Cut-Off and DV Details The Railway Recruitment Board (RRB) has released the RRB Paramedical Score Card 2026 for the CEN 03/2025 Paramedical CBT Exam. Along [...]
RPSC APO Recruitment 2026: Apply for 371 Posts
Mission Gyan2026-05-29T13:23:25+05:30May 29, 2026|2 Comments
RPSC APO Recruitment 2026 Rajasthan Public Service Commission has released the RPSC APO Recruitment 2026 notification for the post of Assistant Prosecution Officer. This recruitment is a good opportunity for law graduates who want a [...]
RPSC 1st Grade Admit Card 2026 Out: Download Link
Mission Gyan2026-05-29T12:24:31+05:30May 29, 2026|0 Comments
RPSC 1st Grade Admit Card 2026 Out ✅ The Rajasthan Public Service Commission has released the RPSC 1st Grade Admit Card 2026 for the School Lecturer / 1st Grade Teacher Exam. Candidates who applied for [...]
UPSC Prelims Answer Key 2026 Out: GS & CSAT PDF
Mission Gyan2026-05-28T12:21:14+05:30May 28, 2026|0 Comments
UPSC Prelims Answer Key 2026 Out: GS & CSAT PDF Released The UPSC Prelims Answer Key 2026 is now available for the Civil Services Preliminary Examination. Candidates who appeared in the exam can check the [...]
REET 3rd Grade Teacher Result 2026 Out
Mission Gyan2026-05-28T11:22:26+05:30May 28, 2026|1 Comment
REET 3rd Grade Teacher Result 2026 Out Latest Update: The Rajasthan Staff Selection Board (RSSB) has released the REET 3rd Grade Teacher Result 2026 on 27 May 2026. Candidates who appeared in the Rajasthan 3rd [...]
RPSC 1st Grade Exam City 2026 Out
Mission Gyan2026-05-27T14:13:35+05:30May 27, 2026|0 Comments
RPSC 1st Grade Teacher Exam City 2026 Out The RPSC 1st Grade Teacher Exam City 2026 slip is now available online. So, candidates who will appear in the Rajasthan School Lecturer exam can check their [...]
SSC CGL 2026 Notification: 12,256 Vacancies Out
Mission Gyan2026-05-29T11:18:23+05:30May 27, 2026|0 Comments
SSC CGL 2026 Notification Out: 12,256 Vacancies, Dates, Eligibility, Exam Pattern & Salary The SSC CGL 2026 Notification is now out for graduate candidates who want Central Government jobs. This year, the Staff Selection Commission [...]
RRB NTPC Result 2026: Scorecard, Cut Off & Merit List
Mission Gyan2026-05-26T18:18:50+05:30May 26, 2026|0 Comments
RRB NTPC Result 2026 Out: Scorecard, Cut Off & Merit List The RRB NTPC Result 2026 has been released for various regions. Candidates who appeared in the NTPC computer-based examination can now check their qualifying [...]
Rajasthan BSTC Admit Card 2026 Out – Download Now
Mission Gyan2026-05-19T15:24:12+05:30May 19, 2026|0 Comments
Rajasthan BSTC Admit Card 2026 Out – Download Hall Ticket Now The Rajasthan BSTC Admit Card 2026 is now available online. Candidates who applied for the Pre D.El.Ed Exam 2026 can download their hall ticket [...]