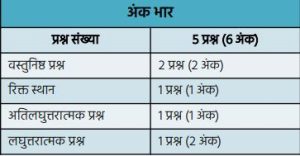
कक्षा 10 विज्ञान अध्याय 1 – रासायनिक अभिक्रियाएँ एवं समीकरण | Class 10 Science Chapter 1 Notes
महत्त्वपूर्ण बिन्दु/ सार
- हमारे चारों ओर प्रतिदिन अनेक प्रकार के परिवर्तन होते रहते हैं — जैसे बर्फ का पिघलना, लोहे में जंग लगना या भोजन का पचना। इन परिवर्तनों में से कुछ केवल भौतिक (Physical) होते हैं, जबकि कुछ रासायनिक (Chemical) होते हैं।
परिवर्तन के प्रकार
भौतिक परिवर्तन रासायनिक परिवर्तन भौतिक परिवर्तन में केवल भौतिक गुणों में परिवर्तन होता है, जैसे — आकार, आकृति, अवस्था। रासायनिक परिवर्तन में पदार्थों के रासायनिक संघटन तथा भौतिक गुणों में परिवर्तन होता है। भौतिक परिवर्तन में कोई नया पदार्थ नहीं बनता है। रासायनिक परिवर्तन में नए पदार्थ का निर्माण होता है। सामान्यतः ये परिवर्तन उत्क्रमणीय (अस्थायी) होते हैं, जैसे — बर्फ का पिघलना, पानी का जमना आदि। ये परिवर्तन अनुत्क्रमणीय (स्थायी) होते हैं, जैसे —
भोजन का पाचन, कोयले का जलना, जंग लगना आदि।
🧪 क्रियाकलाप
🧪क्रियाकलाप 1.1
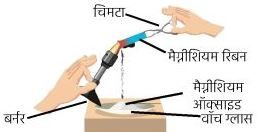
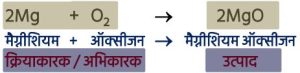
➢ मैग्नीशियम रिबन को वायु में जलाने पर वॉच ग्लास में मैग्नीशियम ऑक्साइड प्राप्त होता है।
🧪क्रियाकलाप 1.2
➢ एक परखनली में लेड (सीसा) नाइट्रेट के घोल की अभिक्रिया पोटैशियम आयोडाइड के घोल से करने पर लेड आयोडाइड का पीला अवक्षेप प्राप्त होता है।
🧪क्रियाकलाप 1.3
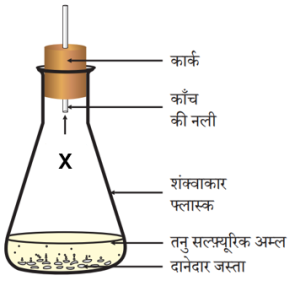
➢ दानेदार जस्ता पर पतला सल्फ्यूरिक अम्ल की अभिक्रिया से हाइड्रोजन गैस का निर्माण होता है।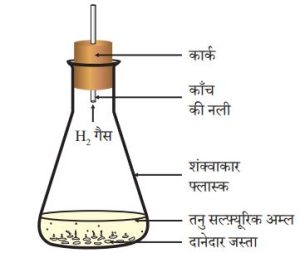
रासायनिक समीकरण
➢ रासायनिक अभिक्रिया के दौरान दो या दो से अधिक पदार्थ आपस में अभिक्रिया करके पूर्णतः भिन्न गुणों वाला नया पदार्थ बनाते हैं। इस प्रकार, नए पदार्थ का निर्माण होता है जो मूल पदार्थों से अलग होता है।
➢रासायनिक अभिक्रियाओं को रासायनिक समीकरण के रूप में लिखा जाता है।
➢किसी रासायनिक अभिक्रिया का प्रतीकों के रूप में निरूपण रासायनिक समीकरण कहलाता है।
➢रासायनिक अभिक्रिया में भाग लेने वाले पदार्थ अभिकारक तथा अभिक्रिया के परिणामस्वरूप बनने वाले नए पदार्थ उत्पाद कहलाते हैं।
➢ रासायनिक समीकरण में अभिकारकों को तीर के निशान के बाईं ओर (LHS) तथा उत्पादों को तीर के निशान के दाईं ओर (RHS) लिखा जाता है।
⚖️ संतुलित रासायनिक समीकरण
➢संतुलित रासायनिक समीकरण में अभिकारकों के परमाणुओं की संख्या तथा उत्पादों के परमाणुओं की संख्या समान होती है। इसलिए, यह सुनिश्चित किया जाता है कि अभिक्रिया में किसी तत्व का न तो ह्रास हो और न ही वृद्धि।
इसके अलावा, द्रव्यमान संरक्षण के नियम के अनुसार, अभिकारकों के तत्वों का कुल द्रव्यमान उत्पादों के तत्वों के कुल द्रव्यमान के समान होना चाहिए।
➢ समीकरण को संतुलित करने के लिए हिट एंड ट्रायल विधि से अभिकारकों और उत्पादों के परमाणुओं की संख्या को बराबर किया जाता है।
➢ समीकरण को अधिक सूचनापूर्ण बनाने के लिए अभिकारकों और उत्पादों की भौतिक अवस्था को भी उनके रासायनिक सूत्रों के साथ दर्शाया जाता है।
➢ कुछ अभिक्रियाओं की परिस्थितियाँ, जैसे ताप, दाब, उत्प्रेरक आदि को भी तीर के निशान के ऊपर या नीचे दर्शाया जाता है।
बहुविकल्पीय प्रश्न
- एक मैग्नीशियम रिबन को हवा में जलाने पर मिलने वाले पाउडर या राख का रंग होता है —
(अ) ग्रे (ब) काला (स) सफेद (द) नीला - Fe + H₂O → Fe₃O₄ + H₂
उपरोक्त अभिक्रिया के संतुलित समीकरण में Fe का गुणांक होगा —
(अ) 1 (ब) 2 (स) 3 (द) 4
दिए गए चित्रानुसार उपरोक्त अभिक्रिया में मिलने वाली गैस X को पहचानिए। (2022)
(अ) O₂ (ब) CO₂ (स) H₂ (द) O₃
बहुविकल्पीय प्रश्नों के हल
(स) सफेद
(ब) 3
(स) H₂
रिक्त स्थान
लेड नाइट्रेट के ऊष्मीय अपघटन से प्राप्त नाइट्रोजन युक्त गैस का नाम …………….. है। (2024)
HCl के अपघटन से प्राप्त ऋणायन का रासायनिक सूत्र …………….. है। (2024)
रिक्त स्थान के हल
लेड नाइट्रेट के ऊष्मीय अपघटन से प्राप्त नाइट्रोजन युक्त गैस का नाम NO₂ है।
HCl के अपघटन से प्राप्त ऋणायन का रासायनिक सूत्र Cl⁻ है।
अति लघुत्तरात्मक प्रश्न
कार्बन के पूर्ण दहन से प्राप्त गैस का नाम लिखिए।
निम्न शब्द समीकरणों को रासायनिक समीकरण के रूप में दर्शाइए —
(i) जिंक + सल्फ्यूरिक अम्ल → जिंक सल्फेट + हाइड्रोजन
(ii) मैग्नीशियम + ऑक्सीजन → मैग्नीशियम ऑक्साइडकिन प्रेक्षणों की सहायता से हम कह सकते हैं कि रासायनिक अभिक्रिया संपन्न हुई है?
द्रव्यमान के संरक्षण के नियम को लिखिए।
संतुलित रासायनिक समीकरण किसे कहते हैं?
अति लघुत्तरात्मक प्रश्नों के हल
CO₂
(i) Zn + H₂SO₄ → ZnSO₄ + H₂
(ii) 2Mg + O₂ → 2MgOरंग में परिवर्तन, अवस्था में परिवर्तन, तापमान में परिवर्तन, गैस का निष्कासन या उत्सर्जन।
किसी भी रासायनिक अभिक्रिया में द्रव्यमान न तो उत्पन्न होता है और न ही नष्ट होता है — यही द्रव्यमान संरक्षण का नियम है।
वह रासायनिक समीकरण जिसमें विभिन्न तत्वों के परमाणुओं की संख्या अभिकारक और उत्पाद, दोनों पक्षों में समान हो, संतुलित रासायनिक समीकरण कहलाता है।
लघुत्तरात्मक प्रश्न
रासायनिक समीकरण की विशेषताएँ बताइए।
वायु में जलाने से पहले मैग्नीशियम रिबन को साफ़ क्यों किया जाता है?
निम्नलिखित रासायनिक अभिक्रियाओं के लिए संतुलित समीकरण लिखिए —
(i) हाइड्रोजन + क्लोरीन → हाइड्रोजन क्लोराइड
(ii) बेरियम क्लोराइड + एल्युमिनियम सल्फेट → बेरियम सल्फेट + एल्युमिनियम क्लोराइड
(iii) सोडियम + जल → सोडियम हाइड्रॉक्साइड + हाइड्रोजननिम्नलिखित अभिक्रियाओं के लिए उनकी अवस्था के संकेतों के साथ संतुलित रासायनिक समीकरण लिखिए—
(i) जल में बेरियम क्लोराइड तथा सोडियम सल्फेट के विलयन अभिक्रिया करके सोडियम क्लोराइड का विलयन तथा अघुलनशील बेरियम सल्फेट का अवक्षेप बनाते हैं।
(ii) सोडियम हाइड्रॉक्साइड का विलयन (जल में) हाइड्रोक्लोरिक अम्ल के विलयन (जल में) से अभिक्रिया करके सोडियम क्लोराइड का विलयन तथा जल बनाते हैं।
- मैग्नीशियम रिबन का वायु में दहन कर वॉच ग्लास में इकट्ठे होने वाले उत्पाद के नाम सहित चित्र बनाइए। (2022)
लघुत्तरात्मक प्रश्न
- रासायनिक समीकरण की विशेषताएँ —
➢ इसके द्वारा अभिकारक एवं उत्पाद के बारे में जानकारी प्राप्त होती है, एवं इनके द्रव्यमान एवं अणुओं की संख्या की जानकारी भी प्राप्त होती है।
➢ पदार्थों की भौतिक अवस्था का पता चलता है।
➢ रासायनिक अभिक्रिया के तापमान एवं दाब की सूचना प्राप्त होती है।
➢ रासायनिक अभिक्रिया में प्रयुक्त उत्प्रेरक की जानकारी प्राप्त होती है।
➢ अभिक्रिया की उत्क्रमणीयता के बारे में जानकारी प्राप्त होती है।
➢ अभिक्रिया में उत्पन्न या प्रयुक्त ऊष्मा के बारे में सूचना प्राप्त होती है।
2.मैग्नीशियम को लंबे समय तक हवा में रखने पर मैग्नीशियम पर ऑक्सीजन की एक परत चढ़ जाती है। यह परत मैग्नीशियम के जलने में बाधा डालती है। इसलिए, इसे जलाने से पहले रेगमाल से साफ करना चाहिए।
3.(i) H₂ + Cl₂ → 2HCl
(ii) 3BaCl₂ + Al₂(SO₄)₃ → 3BaSO₄ + 2AlCl₃
(iii) 2Na + 2H₂O → 2NaOH + H₂↑
4.(i) BaCl₂(aq) + Na₂SO₄(aq) → BaSO₄(s)↓ + 2NaCl(aq)
(ii) NaOH(aq) + HCl(aq) → NaCl(aq) + H₂O(l)
5.मैग्नीशियम ऑक्साइड
रासायनिक अभिक्रियाओं के प्रकार
1.संयोजन अभिक्रिया (Combination Reaction) —
ऐसी अभिक्रियाएँ जिनमें दो या दो से अधिक पदार्थ संयोग करके एक ही उत्पाद बनाते है, संयोजन अभिक्रिया कहलाती है।
उदाहरण —
CaO + H₂O → Ca(OH)₂ + ऊष्मा
C + O₂ → CO₂ (कोयले का दहन)
2H₂ + O₂ → 2H₂O (जल का निर्माण)
N₂ + 3H₂ → 2NH₃ + ऊष्मा
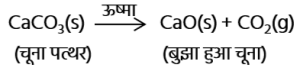
क्रियाकलाप 1.4
जल के साथ कैल्सियम ऑक्साइड की अभिक्रिया से बुझे हुए चूने का निर्माण होता है।
NOTE : कुछ अभिक्रियाओं में उत्पाद के साथ-साथ ऊष्मा भी उत्पन्न होती है, ऐसी अभिक्रियाओं को ऊष्माक्षेपी (Exothermic Reaction) रासायनिक अभिक्रिया कहते है।
उदाहरण —
(i) प्राकृतिक गैस का दहन :
CH₄ + 2O₂(g) → CO₂(g) + 2H₂O + ऊर्जा
(ii) श्वसन :
C₆H₁₂O₆(aq) + 6O₂(aq) → 6CO₂(aq) + 6H₂O(l) + ऊर्जा
(ग्लूकोज)
- श्वसन प्रक्रिया में हमारे शरीर की कोशिकाओं में ग्लूकोज (भोजन से प्राप्त) ऑक्सीजन से क्रिया करता है और ऊर्जा मुक्त करता है।
(iii) शाक सब्जियों (वनस्पतियद्रव्य) का विघटित होकर कंपोस्ट बनना।
NOTE : कुछ अभिक्रियाओं में अभिक्रिया के दौरान ऊष्मा का अवशोषण होता है, ऐसी अभिक्रिया ऊष्माशोषी अभिक्रिया (Endothermic Reaction) कहलाती है।
उदाहरण — N₂(g) + 2O₂(g) + ऊर्जा → 2NO(g)
प्रकाश संश्लेषण : 6CO₂ + 6H₂O → C₆H₁₂O₆ + 6O₂
2. वियोजन अभिक्रिया (Decomposition Reaction) —
- ऐसी अभिक्रिया जिनमें अभिकारक या पदार्थ दो या दो से अधिक सरल अणुओं में अपघटित हो जाता है या टूट जाता है वियोजन अभिक्रिया (अपघटन) कहलाती है।
अपघटन /वियोजन अभिक्रिया के प्रकार
(I) तापीय अपघटन :
- तापीय अपघटन अभिक्रिया में ऊष्मा ऊर्जा का उपयोग होता है।
उदाहरण —
क्रियाकलाप 1.5
- शुष्क क्वथन नली में फेरस सल्फेट के क्रिस्टल को गर्म करने पर हरे रंग का फेरस सल्फेट भूरे रंग के फेरिक ऑक्साइड में परिवर्तित हो जाता है।
उदाहरण —
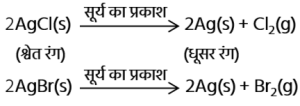
(II) प्रकाश अपघटन :
- प्रकाश अपघटन अभिक्रिया में सूर्य के प्रकाश का उपयोग होता है।
उदाहरण —
सिल्वर क्लोराइड, सिल्वर ब्रोमाइड का अपघटन
NOTE : इस अभिक्रिया का उपयोग श्याम श्वेत फोटोग्राफी (Black and White Photography) में किया जाता है।
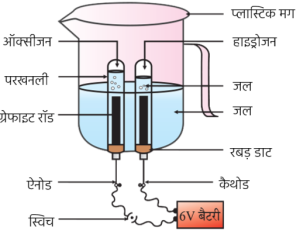
(III) विद्युत अपघटन :
- किसी यौगिक के जलीय विलयन में विद्युत धारा प्रवाहित करने पर वह सरल यौगिकों में टूट जाता है।
उदाहरण —
जल का विद्युत अपघटन
3. विस्थापन व द्विविस्थापन अभिक्रिया —
विस्थापन अभिक्रिया (Displacement Reaction) :
- अभिक्रियाएँ जिनमें अधिक सक्रिय तत्व कम सक्रिय तत्व को विस्थापित कर देता है, विस्थापन अभिक्रिया कहलाती है।
- विस्थापन अभिक्रिया में धातु व अधातु दोनों भाग लेती है।
उदाहरण —
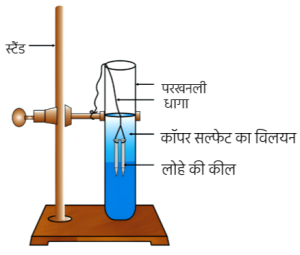
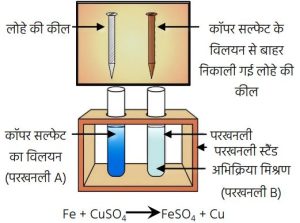
कॉपर सल्फेट के विलयन में डूबी हुई लोहे की कीलें
— याद रखें —
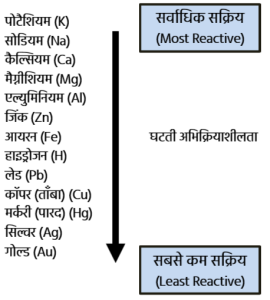
सक्रियता श्रेणी (Reactivity Series) :
- इस श्रेणी में धातुओं को उनके घटती हुई सक्रियता के आधार पर व्यवस्थित किया जाता है।
द्विविस्थापन अभिक्रिया (Double Displacement Reaction) :
- इस प्रकार की अभिक्रिया में दो अभिकारकों के बीच में आयनों का आदान प्रदान होता है और नया पदार्थ (यौगिक) बनता है।
उदाहरण —
| ऑक्सीकरण {(उपचयन) Oxidation} | अपचयन (Reduction) |
| ऑक्सीजन का जुड़ना। | ऑक्सीजन का निकलना। |
| हाइड्रोजन का निकलना। | हाइड्रोजन का जुड़ना। |
| विद्युतऋणी परमाणु का जुड़ना। | विद्युतऋणी परमाणु का निकलना। |
| विद्युतधनी परमाणु का निकलना। | विद्युतधनी परमाणु का जुड़ना। |
| e– का निकलना (इलेक्ट्रॉन) | e– का जुड़ना (गृहण करना) |
| उदाहरण : 2Cu + O2 → 2CuO Fe + S → FeS H2 S + Br2 → 2HBr + S | उदाहरण : CuO + H2 → Cu + H 2O 2FeCl 3 + H 2 → 2FeCl 2 + 2HCl Cu 2+ e e– → Cu(s) |
रेडॉक्स अभिक्रिया (Redox Reaction) :
- वह अभिक्रिया जिसमें ऑक्सीकरण व अपचयन दोनों साथ-साथ होती है।
अथवा
- वे सभी अभिक्रियाएँ जिनमें दो प्रजातियों (यौगिकों) के बीच इलेक्ट्रॉन का आदान प्रदान होता है या परमाणुओं की ऑक्सीकरण अवस्था बदल जाती है।
बहुचयनात्मक प्रश्न
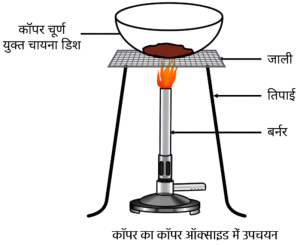
1. तांबा और ऑक्सीजन के मध्य रासायनिक अभिक्रिया, किस अभिक्रिया का उदाहरण है:
(अ) संयोजन अभिक्रिया
(ब) अपघटन अभिक्रिया
(स) विस्थापन अभिक्रिया
(द) उपरोक्त में से कोई नहीं
2. लैंड आयोडाइड का पीला अवक्षेप प्राप्त करने के लिए पोटैशियम आयोडाइड को अभिकृत कराया जाता है?
(अ) लेड सल्फाइड
(ब) लेड नाइट्रेट
(स) पोटैशियम नाइट्रेट
(द) लेड क्लोराइड
3. नीचे दी गई अभिक्रिया के संबंध में कौन सा कथन असत्य है?
2PbO(s) + C(s) → 2Pb(s) + CO2(g)
(a) सीसा अपचयित हो रहा है।
(b) कार्बन डाइऑक्साइड उपचयित हो रहा है।
(c) कार्बन उपचयित हो रहा है।
(d) लेड ऑक्साइड अपचयित हो रहा है।
(अ) (a) एवं (b)
(ब) (a) एवं (c)
(स) (a), (b) एवं (c)
(द) सभी
4. Fe2O3 + 2Al + Al2O3 + 2Fe
ऊपर दी गई अभिक्रिया किस प्रकार की है-
(अ) संयोजन अभिक्रिया
(ब) द्विविस्थापन अभिक्रिया
(स) वियोजन अभिक्रिया
(द) विस्थापन अभिक्रिया
बहुचयनात्मक प्रश्न के हल
1. (अ) संयोजन अभिक्रिया
2. (ब) लेड नाइट्रेट
3. (अ) (a) एवं (b)
4. (द) विस्थापन अभिक्रिया
अतिलघुत्तरात्मक प्रश्न
उपरोक्त अभिक्रिया में अपचयित होने वाले अभिकारक का नाम लिखिए। (2023)
2. C6H12O6 + 6O2 → A + 6H2O से प्राप्त A यौगिक है।
3. किसी पदार्थ ‘X’ के विलयन का उपयोग सफेदी करने के लिए होता है।
(i) पदार्थ ‘X’ का नाम तथा इसका सूत्र लिखिए।
(ii) ऊपर (i) में लिखे पदार्थ ‘X’ की जल के साथ अभिक्रिया लिखिए
4. जब लोहे की कील को कॉपर सल्फेट के विलयन में डुबोया जाता है तो विलयन का रंग क्यों बदल जाता है?
5. भिन्न द्विविस्थापन अभिक्रिया का एक उदाहरण दीजिए।
6. निम्न अभिक्रियाओं में उपचयित तथा अपचयित पदार्थों की पहचान कीजिए —
(i) 4Na(s) + O2(g) → 2Na2O(s)
(ii) CuO(s) + H2(g) → Cu(s) + H2O2(l)
7. ऊष्माशोषी और ऊष्माक्षेपी अभिक्रियाओं को परिभाषित कीजिए। (2022)
8. निम्नलिखित में से प्रत्येक को एक उदाहरण देकर समझाइए — (2023)
(i) संयोजन अभिक्रिया; (ii) वियोजन अभिक्रिया
9. (i) ऑक्सीकरण (उपचयन) अभिक्रिया को उदाहरण सहित समझाइये। (2022)
(ii) निम्नलिखित रासायनिक समीकरण को संतुलित कीजिए।
NH3 + CuO → Cu + N2 + H2O
10. (i) अपचयन अभिक्रिया को उदाहरण सहित समझाइये। (2022)
(ii) निम्नलिखित रासायनिक समीकरण को संतुलित कीजिए।
NaOH + H2SO4 → Na2SO4 + H2O
11. ऑक्सीकरण व अपचयन अभिक्रियाओं को संयुक्त रूप से किस नाम से जानते हैं?
12. पानी के इलेक्ट्रोलिसिस की प्रक्रिया के दौरान ऑक्सीजन गैस कहाँ उत्पन्न होती है?
13. पानी के इलेक्ट्रोलिसिस की प्रक्रिया में हाइड्रोजन गैस कहाँ जमा होती है?
14. अपघटन अभिक्रिया कितने प्रकार की होती हैं?
15. जल के निर्माण के लिए संयोजन अभिक्रिया लिखिए।
16. रासायनिक समीकरण में (↑) एवं (↓) क्या प्रदर्शित करता है?
17. दी गई अभिक्रिया किस प्रकार की है —
Na2SO4 + BaCl2 + BaSO4 + 2NaCl
18. जंग लगने के लिए आवश्यक कारक कौन-कौनसे हैं?
19. भोजन के पाचन में किसी प्रकार की अभिक्रिया होती हैं?
20. अभिक्रिया 2Kl + Cl2 → 2KCl + l2 में ऑक्सीकारक और अपचायक को बताइये।
21. निम्नलिखित तत्वों को उनकी क्रियाशीलता के बढ़ते हुए क्रम में व्यवस्थित कीजिए।
Cu < Fe < Mg < Ca < K
22. कॉपर सल्फेट के नीले रंग के विलयन में जिंक के टुकडे डालने पर क्या प्रभाव पड़ता है।
लघुत्तरात्मक प्रश्न
- (i) कोयले के दहन से प्राप्त गैस का नाम लिखिए।
(ii) कॉपर (II) ऑक्साइड + हाइड्रोजन → कॉपर + जल
उपरोक्त शब्द-समीकरण के लिए संतुलित रासायनिक समीकरण लिखिए।
(iii) कॉपर के कॉपर ऑक्साइड में अपचयन के प्रदर्शन के लिए व्यवस्थित उपकरण को चित्रित कीजिए।
अथवा
(i) अपचयन को परिभाषित कीजिए।
(ii) आयरन + कॉपर सल्फेट → आयरन सल्फेट + कॉपर
उपरोक्त शब्द-समीकरण के लिए संतुलित रासायनिक समीकरण लिखिए।
(iii) कॉपर सल्फेट के विलयन में डूबी लोहे की कीलों की अभिक्रिया के प्रदर्शन के लिए व्यवस्थित उपकरण को चित्रित कीजिए। (2024)
- ऑक्सीकारक व अपचायक से आप क्या समझते हैं?
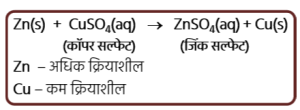
- क्या ये अभिक्रियाएँ संभव हैं? उत्तर कारण सहित लिखिए।
(i) Cu + ZnSO₄ → CuSO₄ + Zn
(ii) Fe + CuSO₄ → FeSO₄ + Cu - एक भूरे रंग का चमकदार धातु ‘X’ को वायु की उपस्थिति में गर्म करने पर वह काले रंग का हो जाता है। इस धातु ‘X’ एवं उस काले रंग के यौगिक का नाम बताइए।
लघुत्तरात्मक प्रश्न के हल
1. (i) C + O₂ → CO₂ कोयले के दहन से कार्बन डाइऑक्साइड गैस प्राप्त होती है
(ii) कॉपर (II) ऑक्साइड + हाइड्रोजन → कॉपर + जल
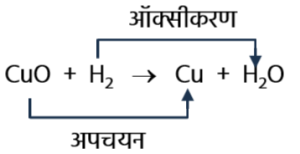
CuO + H₂ → Cu + H₂O
(iii) कॉपर का कॉपर ऑक्साइड में अपचयन
अथवा
(i) अपचयन: वे अभिक्रियाएँ जिनमें ऑक्सीजन का निष्कासन अथवा हाइड्रोजन का योग हो, अपचयन अभिक्रिया कहलाती है।
उदाहरण:
CuO + H₂ → Cu + H₂O
2FeCl₃ + H₂ → 2FeCl₂ + 2HCl
(ii) आयरन + कॉपर सल्फेट → आयरन सल्फेट + कॉपर
(iii) कॉपर सल्फेट के विलयन में डूबी हुई लोहे की कीलें
प्रयोग से पहले तथा उसके उपरांत लोहे की कील तथा कॉपर सल्फेट के विलयन की तुलना
2. ऑक्सीकारक: वे पदार्थ जो स्वयं अपचयित होते हैं तथा अभिक्रिया में उपस्थित दूसरे पदार्थ का ऑक्सीकरण करते हैं, ऑक्सीकारक कहलाते हैं। ऑक्सीकारक में तत्व का ऑक्सीकरण अंक कम होता है।
अपचायक: वे पदार्थ जो इलेक्ट्रॉन देते हैं अर्थात् स्वयं ऑक्सीकरण होते हैं तथा दूसरे पदार्थ का अपचयन करते हैं, अपचायक कहलाते हैं।
उदाहरण:
2HgCl₂ + SnCl₂ → Hg₂Cl₂ + SnCl₄
+2SnCl₂ → +4SnCl₄
Sn का ऑक्सीकरण हो रहा है।
अतः SnCl₂ अपचायक है।
HgCl₂ → Hg₂Cl₂ में अपचयन हो रहा है।
अतः HgCl₂ ऑक्सीकारक है।
3. (i) Cu + ZnSO₄ → CuSO₄ + Zn
(ii) Fe + CuSO₄ → FeSO₄ + Cu
उपरोक्त (i) अभिक्रिया संभव नहीं है, क्योंकि Cu, Zn से कम अभिक्रियाशील है। अतः Cu, Zn धातु को प्रतिस्थापित नहीं कर सकता।
उपरोक्त (ii) अभिक्रिया संभव है, क्योंकि Fe, Cu की अपेक्षा अधिक अभिक्रियाशील है। अतः Fe, Cu धातु को प्रतिस्थापित कर रहा है।
4. भूरे रंग का चमकदार तत्व ‘X’ कॉपर है तथा वायु की उपस्थिति में गर्म करने पर यह काले रंग के यौगिक कॉपर ऑक्साइड में बदल जाता है।![]()
संक्षारण (Corrosion)
वह रासायनिक क्रिया जिसके परिणामस्वरूप धातुओं का क्षय एवं ह्रास होता है, इस प्रकार धातुएँ अपनी चमक और मजबूती खो देती हैं।
➢ जब कोई धातु अपने आस-पास के अम्ल, आद्रता आदि के संपर्क में आती है, तो परिणामस्वरूप वह संक्षारित हो जाती है और यह प्रक्रिया संक्षारण कहलाती है।
उदाहरण — लोहे में जंग लगना।
➢ यह धीमी गति से होने वाली प्रक्रिया है।
➢ इसके कारण कार के ढाँचे, पुल, लोहे की रेलिंग, जहाज तथा धातु विशेषकर लोहे से बनी वस्तुओं की बहुत हानि होती है।
विकृत गंधिता (Rancidity)
वसायुक्त अथवा तैलीय खाद्य सामग्री जब लंबे समय तक रखी रहती है, तो अंततः वह ऑक्सीकरण हो जाती है और उसका स्वाद व गंध परिवर्तित हो जाता है। इसे विकृत गंधिता कहते हैं।
➢ इसीलिए, विकृत गंधिता को रोकने के लिए खाद्य सामग्री को वायुरोधी बर्तनों में रखा जा सकता है तथा उनमें प्रतिऑक्सीकारक पदार्थ मिलाए जाते हैं।
बहुविकल्पीय प्रश्न
- वातावरण में चाँदी के ऊपर काली परत चढ़ने की प्रक्रिया है – (2023)
(अ) अपचयन
(ब) संक्षारण
(स) विकृत गंधिता
(द) द्विविस्थापन - धातु पर जंग को रोकने के लिए किस प्रकार की कोटिंग की जाती है—
(अ) लकड़ी की कोटिंग
(ब) प्लास्टिक की कोटिंग
(स) पेंट और ग्रीस की कोटिंग
(द) केवल जल द्वारा कोटिंग - किस धातु का जंग “गैल्वनाइजिंग” प्रक्रिया से रोका जा सकता है?
(अ) तांबा
(ब) आयरन
(स) जस्ता
(द) सोना
बहुविकल्पीय प्रश्न के हल
- (ब) संक्षारण
- (स) पेंट और ग्रीस की कोटिंग
- (ब) आयरन
अल्पउत्तरात्मक प्रश्न
- विकृत गंधिता के कारण किस प्रकार की गंध उत्पन्न होती है?
- विकृत गंधिता को कैसे रोका जा सकता है?
अल्पउत्तरात्मक प्रश्न के हल
- तेल या वसा में खराब गंध उत्पन्न होती है।
- विकृत गंधिता को कम करने के लिए खाद्य पदार्थों को वायुरोधी बर्तनों में रखना और ठंडे स्थान पर रखना चाहिए।
लघुत्तरात्मक प्रश्न
- लोहे की वस्तुओं को हम पेंट क्यों करते हैं?
- तेल एवं वसायुक्त खाद्य पदार्थों को नाइट्रोजन से प्रभावित क्यों किया जाता है?
- निम्न पदों का वर्णन कीजिए तथा प्रत्येक का एक-एक उदाहरण दीजिए —
(i) संक्षारण
(ii) विकृत गंधिता
लघुत्तरात्मक प्रश्न के हल
- लोहे की वस्तुओं पर ऑक्सीजन व नमी की उपस्थिति में जंग लग जाती है। अतः लोहे की वस्तुओं को वायु व जल के संपर्क में आने से रोकने के लिए उन पर पेंट कर दिया जाता है, ताकि वे लंबे समय तक सुरक्षित रह सकें।
- नाइट्रोजन कम सक्रिय गैस है तथा यह खाद्य पदार्थों को ऑक्सीकरण होने से बचाती है। इसलिए तेल एवं वसायुक्त खाद्य पदार्थों के पैकेट में नाइट्रोजन गैस भरी जाती है, ताकि उनका अपचयन न हो सके।
- (i) संक्षारण — जब कोई धातु अपने आसपास अम्ल, आद्रता आदि के संपर्क में आती है, तो यह संक्षारित हो जाती है। इस प्रक्रिया को संक्षारण कहते हैं।
उदाहरण : लोहे पर जंग लगना, चाँदी पर काली परत चढ़ना।
(ii) विकृत गंधिता — तेल व वसा युक्त खाद्य सामग्री को लंबे समय तक रखने पर वे विकृत गंधित हो जाते हैं, अर्थात् उनके स्वाद व गंध बदल जाते हैं।
उदाहरण : पकी हुई सब्जियों को खुला छोड़ने पर उनका खराब हो जाना अर्थात् उनके स्वाद व गंध में परिवर्तन हो जाना।
RECENT POSTS
UPSSSC Lekhpal Result 2026 Out – Check PDF & Cutoff
Mission Gyan2026-02-27T18:12:57+05:30February 27, 2026|0 Comments
UPSSSC Lekhpal Result 2026 Released The Uttar Pradesh Subordinate Services Selection Commission (UPSSSC) has officially declared the UPSSSC Lekhpal Result 2026 on its website. Candidates who appeared in the exam can now verify whether they [...]
DSSSB ASO Syllabus 2026: Exam Pattern, Syllabus & Tips for Success
Mission Gyan2026-02-26T18:14:56+05:30February 26, 2026|0 Comments
DSSSB ASO Syllabus & Exam Pattern 2026-Complete Guide The Delhi Subordinate Services Selection Board (DSSSB) has announced the syllabus and exam pattern for the Assistant Section Officer (ASO) 2026 exam. Whether you're a first-time candidate [...]
NCERT Class 6 History Ch 6 Answers – Q&A Format
Mission Gyan2026-02-25T23:46:58+05:30February 25, 2026|0 Comments
NCERT Class 6 History Ch 6 Answers The Beginnings of Indian Civilisation (Question–Answer) These NCERT Class 6 History Ch 6 answers are written in simple question-answer format to help students revise quickly and prepare confidently [...]
RBI Office Attendant Admit Card 2026 Out Today – Direct Download Link @ rbi.org.in
Mission Gyan2026-02-24T21:05:42+05:30February 24, 2026|1 Comment
RBI Office Attendant Admit Card 2026 Download Link Active Now The Reserve Bank of India released the RBI Office Attendant Admit Card 2026 on 23 February 2026 on its official website rbi.org.in. Now candidates can [...]
UPSC 2026 Form Last Date Today — Don’t Miss Your Attempt
Mission Gyan2026-02-24T19:02:31+05:30February 24, 2026|0 Comments
UPSC 2026 Last Date Today (Quick Summary) The UPSC 2026 last date to submit the Civil Services Examination form is today. Thousands of aspirants lose their attempt every year simply because they delay filling the [...]
GATE Response Sheet 2026 PDF Download & Score Check
Mission Gyan2026-02-23T18:41:05+05:30February 23, 2026|0 Comments
GATE Response Sheet 2026 PDF Download & Score Check The GATE Response Sheet 2026 PDF has been released on 22 February 2026 on the GOAPS portal. Candidates can now download their recorded responses, compare them [...]
UPSC CAPF AC 2026 Notification – 349 Posts Apply Online
Mission Gyan2026-02-21T20:28:21+05:30February 21, 2026|0 Comments
UPSC CAPF AC 2026 Notification Released The UPSC CAPF AC 2026 notification has been officially released by the Union Public Service Commission. This examination recruits candidates for the post of Assistant Commandant (Group A Officer) [...]
CMAT 2026 Result OUT Live: Download Scorecard & Cutoff
Mission Gyan2026-02-19T20:57:49+05:30February 19, 2026|1 Comment
CMAT 2026 Result OUT! Check Your Percentile & Download Scorecard Now The National Testing Agency (NTA) has officially released the CMAT 2026 result on 17 February 2026. Candidates who appeared for the exam on 25 [...]
CTET Answer Key 2026 LIVE: Response Sheet & Objection Link
Mission Gyan2026-02-19T20:32:45+05:30February 19, 2026|0 Comments
When Will CTET Answer Key 2026 Release? Check Marks & Direct Link The CTET Answer Key 2026 for the February session is expected soon on the official website ctet.nic.in. Candidates who appeared in Paper I [...]
SSC GD Exam Postponed 2026 — Official Notice
Mission Gyan2026-02-19T20:34:03+05:30February 18, 2026|0 Comments
🚨SSC GD Exam Postponed 2026 — Official Notice The Staff Selection Commission (SSC) has officially postponed the SSC GD Constable CBT Exam 2026. The exam was scheduled from 23 February 2026, but will now be [...]